Samenvatting CEL (boek: the cell essentials)
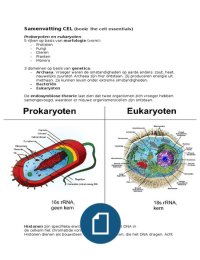
Prokaryoten en eukaryoten
5 rijken op basis van morfologie (vorm):
- Protisten
- Fungi
- Dieren
- Planten
- Monera
3 domeinen op basis van genetica:
- Archaea. Vroeger waren de omstandigheden op aarde anders: zout, heet,
nauwelijks zuurstof. Archaea zijn hier ontstaan. Zij produceren energie uit
methaan. Ze kunnen leven onder extreme omstandigheden.
- Bacteriën
- Eukaryoten
De endosymbiose theorie laat zien dat twee organismen zich vroeger hebben
samengevoegd, waardoor er nieuwe organismen/cellen zijn ontstaan.
Histonen zijn specifieke eiwitten die samen met het DNA in
de celkern het chromatide vormen.
Histonen dienen als bouwsteen voor de nucleosomen, die het DNA dragen. Acht
,histonen vormen een eiwitbolletje, dat een kern vormt waar omheen het lange
DNA-molecuul is gewonden. Ze spelen een belangrijke rol bij het samentrekken
(condenseren) van het DNA tijdens de celkern-deling.
Intronen coderen niet voor een eiwit, extronen wel. Bacteriën hebben geen
intronen.
Bij de RNA polymerases zit er een groot verschil tussen bacteriën en eukaryoten.
Eukaryoten hebben 3 polymerases, bacteriën 1. Die van bacteriën zijn
eenvoudiger in structuur.
*eiwitsynthese (zie GEN jaar 1)
Antibiotica haakt vaak in op het principe van de werking van ribosomen/op het
principe van eiwitsynthese. Hierdoor wordt de eiwitsynthese verstoord.
Het flagel van een prokaryoot is van belang voor beweging. Ook eukaryote
cellen kunnen een flagel hebben. Antibiotica haakt ook in op het flagel, zodat de
bacterie geremd wordt. En flagel komt voor in verschillende
verschijningsvormen. Antibiotica werkt dus in op verschillende prokaryote
eiwitten en mechanismen.
Metabolisme
Metabolisme (stofwisseling) is de overkoepelende naam voor twee processen:
katabolisme (afbraak) en anabolisme (opbouw). Bij katabolisme worden
grote moleculen afgebroken tot kleine moleculen, waarbij energie vrijkomt. Voor
anabolisme is juist energie nodig.
Redoxreacties geven elektronen over. Deze elektronen gaan van een molecuul
met een hoog energieniveau naar een molecuul met een laag energieniveau.
Hierbij verliezen de elektronen dus energie: vrije energie. Deze energie kan
gebruikt worden.
Oxidatie is het verliezen van elektronen (oxidatie = reductor wordt oxidator,
dus verliest zijn elektronen). Reductie is het opnemen van elektronen (reductie
= oxidator wordt reductor, dus neemt elektronen op). Een molecuul dat zijn
elektronen wil afgeven heet een reducerend molecuul. Is het reducerend
molecuul z’n elektronen kwijt, dan is het een geoxideerd molecuul geworden.
Dus: Als je gereduceerd wordt, ontvang je elektronen en als je geoxideerd wordt,
geef je elektronen af.
Een redoxreactie verloopt alleen als er meer vrije energie vrijkomt dan dat er
vrije energie ingestoken moet worden. Vrije energie wordt weergegeven in
‘delta’ Gibbs. Dit moet altijd negatief zijn, aangezien je dan dus netto vrije
energie hebt verloren. Deze vrijgekomen energie kun je dan immers gebruiken.
Reacties op cellulair niveau verlopen dus omdat er meer energie
vrijkomt dan dat er in is gestopt.
De cel ademhaling (metabolisme) bestaat uit 3 stappen:
- Glycolyse
- Citroenzuurcyclus
- Oxidatieve fosforylering
Bij glycolyse en bij de citroenzuurcyclus worden elektronen “omgezet” in NADH
en FADH2.
,Bij de oxidatieve fosforylering worden NADH en FADH 2 “omgezet” in ATP.
Glycolyse
Glycolyse levert energie (waarvan gelijk ATP gemaakt wordt) en geeft de
elektronen die daarbij vrijkomen aan NAD+. Tijdens de glycolyse wordt glucose
omgezet in 2 pyruvaat (C3H6O3) moleculen (+H2O). Dit gebeurt in 10 stappen:
1. Hexokinase: fosfaatgroep van ATP bindt zich aan de glucose. ATP wordt
ADP.
2. Phosphogluco isomerase: glucose (6-ring) wordt fructose (5-ring).
3. Phosphofructokinase: fosfaatgroep van ATP bindt zich aan de fructose.
ATP wordt ADP.
4. Aldolase: fructose (met 2 fosfaten) splitst zich in 2 delen/moleculen:
alleen glyceraldehyde-3-phosphate kan verder reageren.
5. Isomerase: het andere molecuul ontstaan uit de aldolase wordt ook
omgezet in glyceraldehyde-3-phosphate.
6. Troise phosphate dehydrogenase: NAD+ neemt e- op, waardoor er
NADH en H+ ontstaat (bij deze reactie is dus water betrokken). Ook
worden er fosfaatgroepen aan het glyceraldehyde-3-phosphate
gebonden (vrije fosfaatgroepen).
7. Phosphoglycerokinase: een fosfaatgroep koppelt zich los. ADP wordt
ATP.
8. Phosphoglyceromutase: het molecuul verandert van vorm.
9. Enolase: water splitst zich af
10.Pyruvate kinase: een fosfaatgroep koppelt zich los. ADP wordt ATP.
Netto levert de glycolyse dus 2 pyruvaat moleculen, 2 H 2O, 2 ATP en 2 NADH + 2
H+. De pyruvaat gaat de citroenzuurcyclus in.
Citroenzuurcyclus (Krebs cyclus)
Het belangrijkste doel van de citroenzuurcyclus is de productie van NADH. In de
citroenzuurcyclus wordt de oxidatie van de glucose (nu pyruvaat) afgemaakt. De
pyruvaat uit de glycolyse gaat via de preparatory step het mitochondrion in:
Pyruvaat + CoA Acetyl-CoA + CO2. Dit levert 2 NADH.
De citroenzuurcyclus: Het Acetyl-CoA (C2) wordt omgezet in een C6: citrate.
Citrate is het begin en het eindpunt. De cyclus bestaat uit 8 stappen. Er komen in
totaal 2 ATP, 6 NADH en 2 FADH2 vrij. Elke NADH levert 3 ATP op. Elke FADH2
levert 2 ATP op.
Oxidatieve fosforylering
Alle elektronen moeten naar O2 gaan. Dit gaat via de
elektronentransportketen. De elektronentransportketen bestaat uit 4
eiwitcomplexen. De prothetische groepen van deze eiwitcomplexen zorgen
voor het transport van elektronen.
Complex I: NADH geeft zijn elektronen af aan de eiwitten en wordt NAD +.
Complex II: FADH2 geeft zijn elektronen af aan de eiwitten en wordt FAD
Complex IV: geeft 2 elektronen af aan zuurstof, waarna zuurstof samen met H +
wordt omgezet in H2O
,Complex I, III en IV zijn de complexen die H + naar buiten pompen
Het membraan is gerimpeld zodat er meer oppervlak is, waardoor er meer
complexen in passen. Hierdoor kun je dus meer energie vrijmaken.
Door de oxidatie van NADH komt er NAD+, H+ en 2 e- vrij. De 2 e- die vrijkomen
worden opgenomen door de eiwitten in het binnenste membraan van de
mitochondrion. De H+ komt in de intermembrane ruimte (ruimte tussen
binnenste en buitenste membraan). Bij de oxidatie van FADH 2 komt er 2 H+ en 2e-
vrij. De 2 e- gaan naar de eiwitten, de 2 H + naar de intermembrane ruimte.
De 2 e- die zijn “opgeslagen” in de eiwitten worden gebruikt bij de reactie 2 H + +
½ O2 H2O. Bij deze reactie komt er opnieuw een H + terecht in de
intermembrane ruimte. elektronentransportketen
De H+ uit de intermembrane ruimte valt terug en zorgt ervoor dat ADP wordt
omgezet in ATP. In de intermembrane ruimte is de concentratie namelijk hoger,
waardoor de H+ terugvalt. Dit gaat via een “molentje”: ATP synthase. Dit
molentje bestaat uit 4 subunits. Elk subunit bestaat uit meerdere polypeptides.
De elektronentransportketen rondt de transport van elektronen af. Door het
draaien van het molentje wordt energie opgewekt. Deze energie wordt gebruikt
bij de omzetting van ADP in ATP. Chemie-osmose
De enige prokaryoot die oxidatieve fosforylering kan zijn gram negatieve
bacteriën, omdat die een binnen en buitenmembraan hebben.
Het metabolische proces levert dus ONGEVEER 38 ATP op. Als je iets uit de
cyclus haalt om verder te gebruiken, kost dit ATP. Maximaal levert het dus 38 ATP
op, maar soms ook minder. Het proces heeft een rendement van 40% (energie
opgeslagen), de overige 60% zorgt dat je lichaamstemperatuur op pijl blijft.
Het probleem van zuurstof bij de oxidatieve fosforylering bij een bacterie, is dat
er superoxide (O2-) en waterstofperoxide (H2O2) wordt gevormd. Daarom heeft
een bacterie bepaalde enzymen, zodat hij deze stoffen kan afbreken.
, Gisting (fermentatie)
Onder normale omstandigheden gaat NADH naar de elektronentransportketen,
waarna er weer NAD+ ontstaat. De reductie tot NAD+ is namelijk nodig voor de
productie van ATP. Als er geen zuurstof is raakt het NAD + op, waardoor er geen
ATP meer gemaakt kan worden. Er vindt dan fermentatie plaats. Hierbij geeft
NADH zijn elektronen af aan pyruvaat (of afgeleiden daarvan).
Er zijn twee soorten fermentatie:
1. Alcohol fermentatie: glucose wordt omgezet in 2 pyruvaat. 2 pyruvaat
splitst 2 CO2 af, waardoor er 2 acetaldehyde ontstaat. Hierna geeft NADH
zijn 2 elektronen en 2 H+ af, waardoor er 2 ethanol ontstaat.
2. Melkzuur fermentatie: glucose wordt omgezet in 2 pyruvaat. Hierna
geeft NADH zijn 2 elektronen en 2 H+ af aan de 2 pyruvaat, waardoor er 2
melkzuur moleculen ontstaan.
Organismen die leven zonder zuurstof gebruiken dus geen O 2 als elektronen
acceptor, maar bijvoorbeeld sulfaat. Bij fermentatie wordt er 2 ATP
geproduceerd. Het voordeel van fermentatie is dus dat je aan alleen glucose
genoeg hebt om energie te krijgen. Je hoeft dus niet op zoek te gaan naar allerlei
andere moleculen om je elektronen kwijt te raken. Het nadeel is de hele lage
hoeveelheid energie die je krijgt.
Biochemische identificatie
De bonte rij is een verzameling buizen met vloeibare en vaste
voedingsbodems. In elke buis zitten verschillende nutriënten (zoals suikers en
stikstofbronnen) die bacteriën biochemisch kunnen omzetten en kunnen
gebruiken voor hun groei. Deze biochemische omzetting kan leiden tot het
uitscheiden van bepaalde producten, welke kunnen zorgen voor een pH of kleur
verandering.
De eerste 6 buizen van de bonte rij bevatten elk 1% Peptonwater (voor aanmaak
eiwitten), Phenolrood (als pH indicator) en één van de volgende suikers (als C-
bron):
- Glucose
- Lactose (glucose gekoppeld aan galactose)
- Maltose (glucose gekoppeld aan glucose)
- Saccharose (glucose gekoppeld aan fructose)
- Xylose (een C5 i.p.v. een C6)
- Mannitol (C6 die op glucose lijkt)
Bij te weinig zuur slaat de pH indicator niet om, aangezien het Pepton het kleine
beetje zuur neutraliseert. De kleuromslag in de buizen zegt dus iets over de
hoeveelheid zuur die geproduceerd wordt en dus iets over de manier waarop de
bacterie stoffen (met name glucose) afbreekt/omzet.
Een bacterie kan alleen fermentatief op een van deze suikers groeien als hij
deze kan omzetten in glucose, zodat hij deze kan afbreken tijdens de glycolyse.
Kan hij glucose niet fermentatief omzetten, dan kan hij ook de andere suikers
niet fermentatief omzetten.
Verder bestaat de bonte rij uit:
- Indol buis: toont de aanwezigheid van het enzym tryptofenase aan,
welke tryptofaan omzet in Indol. Dit is aan te tonen met Kovacs reagens.
Prokaryoten en eukaryoten
5 rijken op basis van morfologie (vorm):
- Protisten
- Fungi
- Dieren
- Planten
- Monera
3 domeinen op basis van genetica:
- Archaea. Vroeger waren de omstandigheden op aarde anders: zout, heet,
nauwelijks zuurstof. Archaea zijn hier ontstaan. Zij produceren energie uit
methaan. Ze kunnen leven onder extreme omstandigheden.
- Bacteriën
- Eukaryoten
De endosymbiose theorie laat zien dat twee organismen zich vroeger hebben
samengevoegd, waardoor er nieuwe organismen/cellen zijn ontstaan.
Histonen zijn specifieke eiwitten die samen met het DNA in
de celkern het chromatide vormen.
Histonen dienen als bouwsteen voor de nucleosomen, die het DNA dragen. Acht
,histonen vormen een eiwitbolletje, dat een kern vormt waar omheen het lange
DNA-molecuul is gewonden. Ze spelen een belangrijke rol bij het samentrekken
(condenseren) van het DNA tijdens de celkern-deling.
Intronen coderen niet voor een eiwit, extronen wel. Bacteriën hebben geen
intronen.
Bij de RNA polymerases zit er een groot verschil tussen bacteriën en eukaryoten.
Eukaryoten hebben 3 polymerases, bacteriën 1. Die van bacteriën zijn
eenvoudiger in structuur.
*eiwitsynthese (zie GEN jaar 1)
Antibiotica haakt vaak in op het principe van de werking van ribosomen/op het
principe van eiwitsynthese. Hierdoor wordt de eiwitsynthese verstoord.
Het flagel van een prokaryoot is van belang voor beweging. Ook eukaryote
cellen kunnen een flagel hebben. Antibiotica haakt ook in op het flagel, zodat de
bacterie geremd wordt. En flagel komt voor in verschillende
verschijningsvormen. Antibiotica werkt dus in op verschillende prokaryote
eiwitten en mechanismen.
Metabolisme
Metabolisme (stofwisseling) is de overkoepelende naam voor twee processen:
katabolisme (afbraak) en anabolisme (opbouw). Bij katabolisme worden
grote moleculen afgebroken tot kleine moleculen, waarbij energie vrijkomt. Voor
anabolisme is juist energie nodig.
Redoxreacties geven elektronen over. Deze elektronen gaan van een molecuul
met een hoog energieniveau naar een molecuul met een laag energieniveau.
Hierbij verliezen de elektronen dus energie: vrije energie. Deze energie kan
gebruikt worden.
Oxidatie is het verliezen van elektronen (oxidatie = reductor wordt oxidator,
dus verliest zijn elektronen). Reductie is het opnemen van elektronen (reductie
= oxidator wordt reductor, dus neemt elektronen op). Een molecuul dat zijn
elektronen wil afgeven heet een reducerend molecuul. Is het reducerend
molecuul z’n elektronen kwijt, dan is het een geoxideerd molecuul geworden.
Dus: Als je gereduceerd wordt, ontvang je elektronen en als je geoxideerd wordt,
geef je elektronen af.
Een redoxreactie verloopt alleen als er meer vrije energie vrijkomt dan dat er
vrije energie ingestoken moet worden. Vrije energie wordt weergegeven in
‘delta’ Gibbs. Dit moet altijd negatief zijn, aangezien je dan dus netto vrije
energie hebt verloren. Deze vrijgekomen energie kun je dan immers gebruiken.
Reacties op cellulair niveau verlopen dus omdat er meer energie
vrijkomt dan dat er in is gestopt.
De cel ademhaling (metabolisme) bestaat uit 3 stappen:
- Glycolyse
- Citroenzuurcyclus
- Oxidatieve fosforylering
Bij glycolyse en bij de citroenzuurcyclus worden elektronen “omgezet” in NADH
en FADH2.
,Bij de oxidatieve fosforylering worden NADH en FADH 2 “omgezet” in ATP.
Glycolyse
Glycolyse levert energie (waarvan gelijk ATP gemaakt wordt) en geeft de
elektronen die daarbij vrijkomen aan NAD+. Tijdens de glycolyse wordt glucose
omgezet in 2 pyruvaat (C3H6O3) moleculen (+H2O). Dit gebeurt in 10 stappen:
1. Hexokinase: fosfaatgroep van ATP bindt zich aan de glucose. ATP wordt
ADP.
2. Phosphogluco isomerase: glucose (6-ring) wordt fructose (5-ring).
3. Phosphofructokinase: fosfaatgroep van ATP bindt zich aan de fructose.
ATP wordt ADP.
4. Aldolase: fructose (met 2 fosfaten) splitst zich in 2 delen/moleculen:
alleen glyceraldehyde-3-phosphate kan verder reageren.
5. Isomerase: het andere molecuul ontstaan uit de aldolase wordt ook
omgezet in glyceraldehyde-3-phosphate.
6. Troise phosphate dehydrogenase: NAD+ neemt e- op, waardoor er
NADH en H+ ontstaat (bij deze reactie is dus water betrokken). Ook
worden er fosfaatgroepen aan het glyceraldehyde-3-phosphate
gebonden (vrije fosfaatgroepen).
7. Phosphoglycerokinase: een fosfaatgroep koppelt zich los. ADP wordt
ATP.
8. Phosphoglyceromutase: het molecuul verandert van vorm.
9. Enolase: water splitst zich af
10.Pyruvate kinase: een fosfaatgroep koppelt zich los. ADP wordt ATP.
Netto levert de glycolyse dus 2 pyruvaat moleculen, 2 H 2O, 2 ATP en 2 NADH + 2
H+. De pyruvaat gaat de citroenzuurcyclus in.
Citroenzuurcyclus (Krebs cyclus)
Het belangrijkste doel van de citroenzuurcyclus is de productie van NADH. In de
citroenzuurcyclus wordt de oxidatie van de glucose (nu pyruvaat) afgemaakt. De
pyruvaat uit de glycolyse gaat via de preparatory step het mitochondrion in:
Pyruvaat + CoA Acetyl-CoA + CO2. Dit levert 2 NADH.
De citroenzuurcyclus: Het Acetyl-CoA (C2) wordt omgezet in een C6: citrate.
Citrate is het begin en het eindpunt. De cyclus bestaat uit 8 stappen. Er komen in
totaal 2 ATP, 6 NADH en 2 FADH2 vrij. Elke NADH levert 3 ATP op. Elke FADH2
levert 2 ATP op.
Oxidatieve fosforylering
Alle elektronen moeten naar O2 gaan. Dit gaat via de
elektronentransportketen. De elektronentransportketen bestaat uit 4
eiwitcomplexen. De prothetische groepen van deze eiwitcomplexen zorgen
voor het transport van elektronen.
Complex I: NADH geeft zijn elektronen af aan de eiwitten en wordt NAD +.
Complex II: FADH2 geeft zijn elektronen af aan de eiwitten en wordt FAD
Complex IV: geeft 2 elektronen af aan zuurstof, waarna zuurstof samen met H +
wordt omgezet in H2O
,Complex I, III en IV zijn de complexen die H + naar buiten pompen
Het membraan is gerimpeld zodat er meer oppervlak is, waardoor er meer
complexen in passen. Hierdoor kun je dus meer energie vrijmaken.
Door de oxidatie van NADH komt er NAD+, H+ en 2 e- vrij. De 2 e- die vrijkomen
worden opgenomen door de eiwitten in het binnenste membraan van de
mitochondrion. De H+ komt in de intermembrane ruimte (ruimte tussen
binnenste en buitenste membraan). Bij de oxidatie van FADH 2 komt er 2 H+ en 2e-
vrij. De 2 e- gaan naar de eiwitten, de 2 H + naar de intermembrane ruimte.
De 2 e- die zijn “opgeslagen” in de eiwitten worden gebruikt bij de reactie 2 H + +
½ O2 H2O. Bij deze reactie komt er opnieuw een H + terecht in de
intermembrane ruimte. elektronentransportketen
De H+ uit de intermembrane ruimte valt terug en zorgt ervoor dat ADP wordt
omgezet in ATP. In de intermembrane ruimte is de concentratie namelijk hoger,
waardoor de H+ terugvalt. Dit gaat via een “molentje”: ATP synthase. Dit
molentje bestaat uit 4 subunits. Elk subunit bestaat uit meerdere polypeptides.
De elektronentransportketen rondt de transport van elektronen af. Door het
draaien van het molentje wordt energie opgewekt. Deze energie wordt gebruikt
bij de omzetting van ADP in ATP. Chemie-osmose
De enige prokaryoot die oxidatieve fosforylering kan zijn gram negatieve
bacteriën, omdat die een binnen en buitenmembraan hebben.
Het metabolische proces levert dus ONGEVEER 38 ATP op. Als je iets uit de
cyclus haalt om verder te gebruiken, kost dit ATP. Maximaal levert het dus 38 ATP
op, maar soms ook minder. Het proces heeft een rendement van 40% (energie
opgeslagen), de overige 60% zorgt dat je lichaamstemperatuur op pijl blijft.
Het probleem van zuurstof bij de oxidatieve fosforylering bij een bacterie, is dat
er superoxide (O2-) en waterstofperoxide (H2O2) wordt gevormd. Daarom heeft
een bacterie bepaalde enzymen, zodat hij deze stoffen kan afbreken.
, Gisting (fermentatie)
Onder normale omstandigheden gaat NADH naar de elektronentransportketen,
waarna er weer NAD+ ontstaat. De reductie tot NAD+ is namelijk nodig voor de
productie van ATP. Als er geen zuurstof is raakt het NAD + op, waardoor er geen
ATP meer gemaakt kan worden. Er vindt dan fermentatie plaats. Hierbij geeft
NADH zijn elektronen af aan pyruvaat (of afgeleiden daarvan).
Er zijn twee soorten fermentatie:
1. Alcohol fermentatie: glucose wordt omgezet in 2 pyruvaat. 2 pyruvaat
splitst 2 CO2 af, waardoor er 2 acetaldehyde ontstaat. Hierna geeft NADH
zijn 2 elektronen en 2 H+ af, waardoor er 2 ethanol ontstaat.
2. Melkzuur fermentatie: glucose wordt omgezet in 2 pyruvaat. Hierna
geeft NADH zijn 2 elektronen en 2 H+ af aan de 2 pyruvaat, waardoor er 2
melkzuur moleculen ontstaan.
Organismen die leven zonder zuurstof gebruiken dus geen O 2 als elektronen
acceptor, maar bijvoorbeeld sulfaat. Bij fermentatie wordt er 2 ATP
geproduceerd. Het voordeel van fermentatie is dus dat je aan alleen glucose
genoeg hebt om energie te krijgen. Je hoeft dus niet op zoek te gaan naar allerlei
andere moleculen om je elektronen kwijt te raken. Het nadeel is de hele lage
hoeveelheid energie die je krijgt.
Biochemische identificatie
De bonte rij is een verzameling buizen met vloeibare en vaste
voedingsbodems. In elke buis zitten verschillende nutriënten (zoals suikers en
stikstofbronnen) die bacteriën biochemisch kunnen omzetten en kunnen
gebruiken voor hun groei. Deze biochemische omzetting kan leiden tot het
uitscheiden van bepaalde producten, welke kunnen zorgen voor een pH of kleur
verandering.
De eerste 6 buizen van de bonte rij bevatten elk 1% Peptonwater (voor aanmaak
eiwitten), Phenolrood (als pH indicator) en één van de volgende suikers (als C-
bron):
- Glucose
- Lactose (glucose gekoppeld aan galactose)
- Maltose (glucose gekoppeld aan glucose)
- Saccharose (glucose gekoppeld aan fructose)
- Xylose (een C5 i.p.v. een C6)
- Mannitol (C6 die op glucose lijkt)
Bij te weinig zuur slaat de pH indicator niet om, aangezien het Pepton het kleine
beetje zuur neutraliseert. De kleuromslag in de buizen zegt dus iets over de
hoeveelheid zuur die geproduceerd wordt en dus iets over de manier waarop de
bacterie stoffen (met name glucose) afbreekt/omzet.
Een bacterie kan alleen fermentatief op een van deze suikers groeien als hij
deze kan omzetten in glucose, zodat hij deze kan afbreken tijdens de glycolyse.
Kan hij glucose niet fermentatief omzetten, dan kan hij ook de andere suikers
niet fermentatief omzetten.
Verder bestaat de bonte rij uit:
- Indol buis: toont de aanwezigheid van het enzym tryptofenase aan,
welke tryptofaan omzet in Indol. Dit is aan te tonen met Kovacs reagens.