Elektromagnetische straling = EM straling
Kan op 2 manieren beschouwd worden:
- Als golfverschijnsel
- Als stroom van energiedeeltjes = fotonen
EM straling als golfverschijnsel
EM = oscillerende elektrische en magnetische velden die
sinusoïdale golven vormen die loodrecht op elkaar staan.
Alleen het elektrische component is verantwoordelijk voor
verschillende fenomenen die we bestuderen.
Belangrijke eigenschappen vd golf:
- Amplitude A = lengte vd elektrische vector in maximum vd golf
- Golflengte = lineaire afstand tussen twee equivalente punten
- Frequentie u = # golven per seconde bepaald door bron
- Golfgetal v = # golven per cm = 1/
- Voortplantingssnelheid u = v en v = u/ = constante
Ze hebben geen medium nodig om zicht voort te bewegen.
In vacuüm = snelst = lichtsnelheid c = 3,00 * 108 m/s
In materie vermindert de voortplantingssnelheid door interactie met de gebonden
elektronen in de materie u < c
brekingsindex n om de golflengte te bepalen
c u .❑ vac ❑vac
n= = =
u u .❑med ❑med
EM straling als energiebron
Wet van Planck zegt dat de hoeveelheid energie evenredig is met de frequentie vd straling:
c
E=hv=h =hc v h = cte van Planck = 6,626.10-34 J.s
❑
Hoeveelheid energie kan uitgedrukt worden in:
−16
- Joule: 1,99.10
❑
8
- Per mol fotonen: 1,20.10
❑
1240
- eV:
❑
- Golfgetal: E(eV) . 8065
Energietoestand in chemische stoffen
Atomen, ionen en moleculen bestaan alleen in enkele discrete toestanden, als een stof van
toestand wijzigt dan gaat dit gepaard met absorptie of emissie ve hoeveelheid energie die
1
,exact gelijk is aan het energieverschil tussen de toestanden. De frequentie of golflengte
c
wordt bepaald door: E=E1−E 0=hv=h
❑
Voor atomen en ionen wordt energie bepaald door de beweging van elektronen rond de kern
elektronenniveau ’s
Moleculen hebben naast elektronenniveau ’s ook vibratieniveau ’s en rotatieniveau ‘s.
Afhankelijk vd vibraties tussen atomen
Afhankelijk vd rotatie ve molecule rond zijn zwaartepunt.
Stralingsprocessen
In spectroscopie wordt info over een analyt bekomen door de interactie met straling te
bestuderen. Staal is aan start in de grondtoestand en wordt door externe stimulus naar een
aangeslagen toestand gebracht = energie onder de vorm van warmte, elektrische energie,
licht of een chemische reactie.
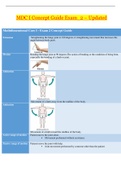
Emissie van straling = emissiespectroscopie
Analyt wordt aangeslagen door warmte, elektrische energie of een chemische
reactie
chemische reactie = chemiluminescentie spectroscopie
Men meet de geëmitteerde straling IE die vrijkomt bij terugkeren naar de
grondtoestand.
er wordt kwalitatieve en kwantitatieve info verzameld
Energieschema: Stippellijn = stralingsloze excitatie proces analyt wordt
oooooooiiiiiiiiiiiiiiiiiiiiiiiiiiiiiiiii aangeslagen naar de 1e of 2e aangeslagen
oooooooiiiiiiiiiiiiiiiiiiiiiiiiiiiiiiiii toestand.
Oooooooiiiiiiiiiii Volle lijn = verlies van energie door emissie ve foton = straling.
Spectrum = geëmitteerde straling uitgezet in functie vd golflengte.
Absorptie van straling = absorptie spectroscopie
Hoeveelheid geadsorbeerde straling meten in functie vd golflengte.
Kwalitatieve en kwantitatieve info
Enkel de fotonen die exact dezelfde energie hebben als het energieverschil
tussen grondtoestand en aangeslagen toestand zullen geabsorbeerd
worden. Dit zijn volle lijnen in het energiediagram
Spectrum = absorptie (A) of transmissie (T) in functie vd golflengte
Luminescentie = fotoluminescentie spectroscopie
Emissie van fotonen gemeten na absorptie van straling. Afhankelijk vd duur vd geëxciteerde
toestand onderscheidt men fluorescentie en fosforescentie. De emissie
wordt loodrecht op de invallende straal gemeten zeker geen uittreden
straling opgemeten.
2
,Volle zwarte pijlen = absorptie van straling gaat naar 1e of 2e aangeslagen toestand.
Terugvallen = emissie ve foton = blauwe lijnen, stralingsloze processen = stippellijn.
Spectrum = intensiteit vd geëmitteerde straling i.f.v. de golflengte.
Types van spectra
- Lijnenspectrum
o Alle lijnen zijn van elkaar gescheiden
o Liggen verspreid over hele golflengtegebied
o Gevolg van elektronentransities in atomen
- Bandenspectrum
o Lijnen zijn gegroepeerd tot banden in bepaalde golflengtegebieden
o Gevolg van elektronentransities in moleculen of atoomgroepen
- Continuüm spectrum
o 1 dikke band over een groot deel vh golflengtegebied.
o Gevolg van gloeiende vaste deeltjes
Lijnenspectra
Baan die elektron in een atoom volgt = beschreven door 4 kwantumgetallen:
- Hoofdkwantumgetal n = energieniveau
- Nevenkwantumgetal l = soort orbitaal
- Magneetkwantumgetal m = oriëntatie vh orbitaal
- Spinkwantumgetal s = rotatierichting
Voorbeeld: natrium: grondtoestand = 1s22s22p63s1
Energieverschil tussen 3s en 3p = 2,105 eV golflengte bepalen die waargenomen wordt als
1240 1240
elektron terugvalt van 3p naar 3s: E= ❑ =2,105 ⟺= =589,07 nm
2,105
Bij deze golflengte zal men de resonantielijn van natrium terugvinden.
Lijn die bekomen wordt door overgang tussen hoogste gevulde en laagste ongevuld
ooooiiiiiii orbitaal. Geeft de hoogste intensiteit en is gevoeligste voor analytische bepalingen.
Het is mogelijk dat een foton wordt geëmitteerd met een andere energie er is niet 1
scherpe lijn met 1 waarde voor maar een zekere breedte en Gausiaanse vorm
Lijnverbreding = veroorzaakt door natuurlijke verbreding.
Bandenspectra
Er zijn ook vibartionele en rotationele energieniveau ’s aanwezig
er zijn een aantal mogelijke golflengtes die overeenkomen met het energieverschil tussen
de verschillende niveau ‘s. bredere piek of band in het spectrum.
- Elektronenniveau ‘s
o Opname ve bepaalde energie e- naar een hoger gelegen molecuulorbitaal.
o Golflengte tussen 666 en 200 nm
- Vibratieniveau ‘s
3
, o Atoomkernen trillen rond evenwichtspositie
o 0,12 eV = 10 333 nm
- Rotatieniveau ‘s
o Moleculen draaien rond as en om eigen bindingen
o 0,1 tot 0,001 eV = 12 400 nm tot 1 240 000 nm
Onderdelen vd apparatuur
= zelf geschreven zie notities
Wet van Lambert-Beer
= zelf geschreven zie notities
UV-VIS spectroscopie
Er wordt gebruik gemaakt van EM straling met golflengte tussen 190 en 800 nm.
Veel gebruikt voor kwantitatieve bepalingen
Instrumentatie
Bestaat uit een stralingsbron, golflengteselectoren, meetcel, detector en computer om data
te lezen.
Meest gebruikte stralingsbronnen:
- Deuteriumlampen 190-400 nm
- Wolfraamlampen 320-2500 nm
- LEDs minder gebruikt, voor bijna monochromatische straling te produceren.
Er kunnen verschillende golflengteselectoren gebruikt worden: absorptiefilters,
interferentiefilters en monochromators.
Meetcellen = fused silica of kwarts, eventueel plastieke meetcellen voor het visuele gebied.
Let op dat de vensters vd meetcel zeer proper zijn beïnvloeden de metingen
Detectoren = fotomultiplicatorbuizen of DAD type arrays meerdere golflengtes simultaan
opmeten.
2 type toestellen:
- Enkele straal toestellen
o Straal wordt niet opgesplitst 1 meetcel simultaan opmeten
- Dubbele straal toestellen
o Straal wordt opgesplitst blanco en staal tegelijk opmeten.
Fotometer
Eenvoudige toestellen waarmee absorptiemetingen kunnen worden uitgevoerd.
Je meet 1 bepaalde golflengte om daar dan een absorbantie van op te meten.
- Visuele fotomoter
4
Kan op 2 manieren beschouwd worden:
- Als golfverschijnsel
- Als stroom van energiedeeltjes = fotonen
EM straling als golfverschijnsel
EM = oscillerende elektrische en magnetische velden die
sinusoïdale golven vormen die loodrecht op elkaar staan.
Alleen het elektrische component is verantwoordelijk voor
verschillende fenomenen die we bestuderen.
Belangrijke eigenschappen vd golf:
- Amplitude A = lengte vd elektrische vector in maximum vd golf
- Golflengte = lineaire afstand tussen twee equivalente punten
- Frequentie u = # golven per seconde bepaald door bron
- Golfgetal v = # golven per cm = 1/
- Voortplantingssnelheid u = v en v = u/ = constante
Ze hebben geen medium nodig om zicht voort te bewegen.
In vacuüm = snelst = lichtsnelheid c = 3,00 * 108 m/s
In materie vermindert de voortplantingssnelheid door interactie met de gebonden
elektronen in de materie u < c
brekingsindex n om de golflengte te bepalen
c u .❑ vac ❑vac
n= = =
u u .❑med ❑med
EM straling als energiebron
Wet van Planck zegt dat de hoeveelheid energie evenredig is met de frequentie vd straling:
c
E=hv=h =hc v h = cte van Planck = 6,626.10-34 J.s
❑
Hoeveelheid energie kan uitgedrukt worden in:
−16
- Joule: 1,99.10
❑
8
- Per mol fotonen: 1,20.10
❑
1240
- eV:
❑
- Golfgetal: E(eV) . 8065
Energietoestand in chemische stoffen
Atomen, ionen en moleculen bestaan alleen in enkele discrete toestanden, als een stof van
toestand wijzigt dan gaat dit gepaard met absorptie of emissie ve hoeveelheid energie die
1
,exact gelijk is aan het energieverschil tussen de toestanden. De frequentie of golflengte
c
wordt bepaald door: E=E1−E 0=hv=h
❑
Voor atomen en ionen wordt energie bepaald door de beweging van elektronen rond de kern
elektronenniveau ’s
Moleculen hebben naast elektronenniveau ’s ook vibratieniveau ’s en rotatieniveau ‘s.
Afhankelijk vd vibraties tussen atomen
Afhankelijk vd rotatie ve molecule rond zijn zwaartepunt.
Stralingsprocessen
In spectroscopie wordt info over een analyt bekomen door de interactie met straling te
bestuderen. Staal is aan start in de grondtoestand en wordt door externe stimulus naar een
aangeslagen toestand gebracht = energie onder de vorm van warmte, elektrische energie,
licht of een chemische reactie.
Emissie van straling = emissiespectroscopie
Analyt wordt aangeslagen door warmte, elektrische energie of een chemische
reactie
chemische reactie = chemiluminescentie spectroscopie
Men meet de geëmitteerde straling IE die vrijkomt bij terugkeren naar de
grondtoestand.
er wordt kwalitatieve en kwantitatieve info verzameld
Energieschema: Stippellijn = stralingsloze excitatie proces analyt wordt
oooooooiiiiiiiiiiiiiiiiiiiiiiiiiiiiiiiii aangeslagen naar de 1e of 2e aangeslagen
oooooooiiiiiiiiiiiiiiiiiiiiiiiiiiiiiiiii toestand.
Oooooooiiiiiiiiiii Volle lijn = verlies van energie door emissie ve foton = straling.
Spectrum = geëmitteerde straling uitgezet in functie vd golflengte.
Absorptie van straling = absorptie spectroscopie
Hoeveelheid geadsorbeerde straling meten in functie vd golflengte.
Kwalitatieve en kwantitatieve info
Enkel de fotonen die exact dezelfde energie hebben als het energieverschil
tussen grondtoestand en aangeslagen toestand zullen geabsorbeerd
worden. Dit zijn volle lijnen in het energiediagram
Spectrum = absorptie (A) of transmissie (T) in functie vd golflengte
Luminescentie = fotoluminescentie spectroscopie
Emissie van fotonen gemeten na absorptie van straling. Afhankelijk vd duur vd geëxciteerde
toestand onderscheidt men fluorescentie en fosforescentie. De emissie
wordt loodrecht op de invallende straal gemeten zeker geen uittreden
straling opgemeten.
2
,Volle zwarte pijlen = absorptie van straling gaat naar 1e of 2e aangeslagen toestand.
Terugvallen = emissie ve foton = blauwe lijnen, stralingsloze processen = stippellijn.
Spectrum = intensiteit vd geëmitteerde straling i.f.v. de golflengte.
Types van spectra
- Lijnenspectrum
o Alle lijnen zijn van elkaar gescheiden
o Liggen verspreid over hele golflengtegebied
o Gevolg van elektronentransities in atomen
- Bandenspectrum
o Lijnen zijn gegroepeerd tot banden in bepaalde golflengtegebieden
o Gevolg van elektronentransities in moleculen of atoomgroepen
- Continuüm spectrum
o 1 dikke band over een groot deel vh golflengtegebied.
o Gevolg van gloeiende vaste deeltjes
Lijnenspectra
Baan die elektron in een atoom volgt = beschreven door 4 kwantumgetallen:
- Hoofdkwantumgetal n = energieniveau
- Nevenkwantumgetal l = soort orbitaal
- Magneetkwantumgetal m = oriëntatie vh orbitaal
- Spinkwantumgetal s = rotatierichting
Voorbeeld: natrium: grondtoestand = 1s22s22p63s1
Energieverschil tussen 3s en 3p = 2,105 eV golflengte bepalen die waargenomen wordt als
1240 1240
elektron terugvalt van 3p naar 3s: E= ❑ =2,105 ⟺= =589,07 nm
2,105
Bij deze golflengte zal men de resonantielijn van natrium terugvinden.
Lijn die bekomen wordt door overgang tussen hoogste gevulde en laagste ongevuld
ooooiiiiiii orbitaal. Geeft de hoogste intensiteit en is gevoeligste voor analytische bepalingen.
Het is mogelijk dat een foton wordt geëmitteerd met een andere energie er is niet 1
scherpe lijn met 1 waarde voor maar een zekere breedte en Gausiaanse vorm
Lijnverbreding = veroorzaakt door natuurlijke verbreding.
Bandenspectra
Er zijn ook vibartionele en rotationele energieniveau ’s aanwezig
er zijn een aantal mogelijke golflengtes die overeenkomen met het energieverschil tussen
de verschillende niveau ‘s. bredere piek of band in het spectrum.
- Elektronenniveau ‘s
o Opname ve bepaalde energie e- naar een hoger gelegen molecuulorbitaal.
o Golflengte tussen 666 en 200 nm
- Vibratieniveau ‘s
3
, o Atoomkernen trillen rond evenwichtspositie
o 0,12 eV = 10 333 nm
- Rotatieniveau ‘s
o Moleculen draaien rond as en om eigen bindingen
o 0,1 tot 0,001 eV = 12 400 nm tot 1 240 000 nm
Onderdelen vd apparatuur
= zelf geschreven zie notities
Wet van Lambert-Beer
= zelf geschreven zie notities
UV-VIS spectroscopie
Er wordt gebruik gemaakt van EM straling met golflengte tussen 190 en 800 nm.
Veel gebruikt voor kwantitatieve bepalingen
Instrumentatie
Bestaat uit een stralingsbron, golflengteselectoren, meetcel, detector en computer om data
te lezen.
Meest gebruikte stralingsbronnen:
- Deuteriumlampen 190-400 nm
- Wolfraamlampen 320-2500 nm
- LEDs minder gebruikt, voor bijna monochromatische straling te produceren.
Er kunnen verschillende golflengteselectoren gebruikt worden: absorptiefilters,
interferentiefilters en monochromators.
Meetcellen = fused silica of kwarts, eventueel plastieke meetcellen voor het visuele gebied.
Let op dat de vensters vd meetcel zeer proper zijn beïnvloeden de metingen
Detectoren = fotomultiplicatorbuizen of DAD type arrays meerdere golflengtes simultaan
opmeten.
2 type toestellen:
- Enkele straal toestellen
o Straal wordt niet opgesplitst 1 meetcel simultaan opmeten
- Dubbele straal toestellen
o Straal wordt opgesplitst blanco en staal tegelijk opmeten.
Fotometer
Eenvoudige toestellen waarmee absorptiemetingen kunnen worden uitgevoerd.
Je meet 1 bepaalde golflengte om daar dan een absorbantie van op te meten.
- Visuele fotomoter
4