Moleculaire celbiologie - H.4 – 15/09/2017
Eiwitten zijn de ‘werkpaarden van het leven’. Eiwitten zijn heel divers. Ze verschillen in
vorm, modulariteit en functie. Alle eiwitten zijn divers, ze veranderen steeds van
samenstelling, maar de bouwstenen voor de samenstellingen zijn al bekend. Verschillende
structuren eiwitten:
Primaire structuur: aminozuurvolgorde
Secundaire structuur: α-helixen en β-sheetshelixen en β-helixen en β-sheetssheets
Backbone: hoofdketen
Side Chain: zijketen
Bindingen secundaire structuur:
Backbone to backbone: waterstofbrug tussen 2 atomen van 2 peptide bindgen
Backbone to side chain: waterstofburg tussen een atoom van een peptidebinding en
een aminozuurzijketen.
Side chain to side chain: waterstofbrug tussen twee aminozuurzijketens
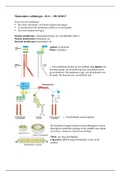
α-helix
α-helix binding: waterstofbrug tussen de N-helixen en β-sheetsH groep van het aminozuurnummer x
met de C=O groep van aminozuurnummer (x+4). Eén hydrofobe kant: (x+3)
hydrofobe aminozuren.
Coiled-coil structuur: α-helixen en β-sheetshelices zijn rond elkaar geregen om de hydrofobe
aminozuren aan de binnenkant te houden.
Amfipatische helix: aan de ene kant van de helix hydrofobe aminozuren en aan de
andere kant hydrofiele aminozuren
α-helixen en β-sheetshelices zijn nodig voor de membraameiwitten.
Je hebt hydrofobe α-helixen en β-sheetshelices nodig om door een membraam heen te komen
β-sheet
Heeft H-helixen en β-sheetsbindingen in de hoofdketen tussen beta-helixen en β-sheetsstrengen.
Aminozuren zitten steeds om en om omdat dat beter is voor de geometrie van de
peptidebinding.
Anti-parallele β-sheet
Parallele β-sheet
Eiwitten zijn de ‘werkpaarden van het leven’. Eiwitten zijn heel divers. Ze verschillen in
vorm, modulariteit en functie. Alle eiwitten zijn divers, ze veranderen steeds van
samenstelling, maar de bouwstenen voor de samenstellingen zijn al bekend. Verschillende
structuren eiwitten:
Primaire structuur: aminozuurvolgorde
Secundaire structuur: α-helixen en β-sheetshelixen en β-helixen en β-sheetssheets
Backbone: hoofdketen
Side Chain: zijketen
Bindingen secundaire structuur:
Backbone to backbone: waterstofbrug tussen 2 atomen van 2 peptide bindgen
Backbone to side chain: waterstofburg tussen een atoom van een peptidebinding en
een aminozuurzijketen.
Side chain to side chain: waterstofbrug tussen twee aminozuurzijketens
α-helix
α-helix binding: waterstofbrug tussen de N-helixen en β-sheetsH groep van het aminozuurnummer x
met de C=O groep van aminozuurnummer (x+4). Eén hydrofobe kant: (x+3)
hydrofobe aminozuren.
Coiled-coil structuur: α-helixen en β-sheetshelices zijn rond elkaar geregen om de hydrofobe
aminozuren aan de binnenkant te houden.
Amfipatische helix: aan de ene kant van de helix hydrofobe aminozuren en aan de
andere kant hydrofiele aminozuren
α-helixen en β-sheetshelices zijn nodig voor de membraameiwitten.
Je hebt hydrofobe α-helixen en β-sheetshelices nodig om door een membraam heen te komen
β-sheet
Heeft H-helixen en β-sheetsbindingen in de hoofdketen tussen beta-helixen en β-sheetsstrengen.
Aminozuren zitten steeds om en om omdat dat beter is voor de geometrie van de
peptidebinding.
Anti-parallele β-sheet
Parallele β-sheet