4.2 Aromaticity
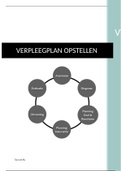
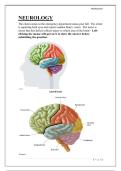
Benzene
• Planar Molecule
• All bond angles are 120
• Each C is bonded to two other carbons and one Hydrogen by sigma (σ)
bonds
• The fourth e- in the 2p orbital above and below the plane is delocalised as
the p orbitals overlap
• Creates a pi (π) electron ring system which is very stable
• Does not undergo addition reactions easily as it would disrupt the πe- ring system
Kekulés Theory
Problem 1 – Reactions of Benzene
• Would expect Kekulés structure of Benzene to react through
electrophilic addition due to double bonds
• This would cause Bromine water to decolourise but it does not
C6H6 + 3Br2 C6H6Br6
• Benzene is relatively unreactive under normal conditions so suggests
no double bonds present
Problem 2 – Thermostability of Benzene
• Enthalpy of hydrogenation to Cyclohexene is -120 KJmol-1
• Enthalpy of hydrogenation to Benzene should be -360 KJmol-1
• Actual enthalpy of hydrogenation of Benzene is -152 KJmol-1 so it is 208 KJmol-1 more stable
, Problem 3 – Bond Lengths
• The bond length of Benzene is between a single and double
Carbon bond suggesting the bonds alternate between carbons
causing resonance.
Reactions of Benzene
• Cannot undergo addition reactions unless vigorous conditions
• πe- ring system is very stable and would be disrupted
• Benzene reacts through electrophilic substitution
Electrophile – An electron deficient species/lone pair acceptor e.g. NO2+, Cl+, CH3+
General Mechanism for Electrophilic Substitution of Benzene
1. The πe- ring system is an area of high e- density and so is attracted to positive electrophile
2. The πe- ring system is disrupted (less stable) with original H and electrophile bonded to C
3. The H leaves and gives the bonded e- back to the πe- ring which is reformed, the H has been
substituted
Benzene
• Planar Molecule
• All bond angles are 120
• Each C is bonded to two other carbons and one Hydrogen by sigma (σ)
bonds
• The fourth e- in the 2p orbital above and below the plane is delocalised as
the p orbitals overlap
• Creates a pi (π) electron ring system which is very stable
• Does not undergo addition reactions easily as it would disrupt the πe- ring system
Kekulés Theory
Problem 1 – Reactions of Benzene
• Would expect Kekulés structure of Benzene to react through
electrophilic addition due to double bonds
• This would cause Bromine water to decolourise but it does not
C6H6 + 3Br2 C6H6Br6
• Benzene is relatively unreactive under normal conditions so suggests
no double bonds present
Problem 2 – Thermostability of Benzene
• Enthalpy of hydrogenation to Cyclohexene is -120 KJmol-1
• Enthalpy of hydrogenation to Benzene should be -360 KJmol-1
• Actual enthalpy of hydrogenation of Benzene is -152 KJmol-1 so it is 208 KJmol-1 more stable
, Problem 3 – Bond Lengths
• The bond length of Benzene is between a single and double
Carbon bond suggesting the bonds alternate between carbons
causing resonance.
Reactions of Benzene
• Cannot undergo addition reactions unless vigorous conditions
• πe- ring system is very stable and would be disrupted
• Benzene reacts through electrophilic substitution
Electrophile – An electron deficient species/lone pair acceptor e.g. NO2+, Cl+, CH3+
General Mechanism for Electrophilic Substitution of Benzene
1. The πe- ring system is an area of high e- density and so is attracted to positive electrophile
2. The πe- ring system is disrupted (less stable) with original H and electrophile bonded to C
3. The H leaves and gives the bonded e- back to the πe- ring which is reformed, the H has been
substituted