Katalyse
4052KATAL
Samenvatting
Pagina 1 van 14
, 4052KATAL SAMENVATTING
Inhoudsopgave
Inhoudsopgave 2
College 1 Inleiding 3
College 2 Heterogene katalyse 5
College 3 Homogene katalyse 7
College 4 Elektrokatalyse 9
College 5 Biokatalyse 11
College 6 Vele wegen naar Rome 13
Pagina 2 van 14
, 4052KATAL SAMENVATTING
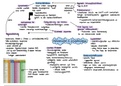
College 1 Inleiding
Katalyse is de versnelling van een traag verlopend chemisch proces door de aanwezigheid van
een vreemde stof. Dit doet een katalysator door het verlagen van de activeringsenergie, vaak door
het stabiliseren van intermediairen. Buiten het versnellen kan katalyse ook een chemische reactie
sturen naar het gewenste eindproduct.
Een katalysator verandert de manier waarop het chemisch evenwicht bereikt wordt, maar niet de
ligging van het evenwicht van de totaalreactie. Dit betekent dat katalyse een kinetisch fenomeen
is en niet thermodynamisch.
Gekatalyseerde reacties zijn vaak ingewikkeld en dan krijg je soms meerdere reactiecoördinaten.
Dan krijg je een meer dimensionale grafiek.
Arrhenius
⎛ E ⎞
k = A exp ⎜ − act ⎟ met k de snelheidsconstante, A een pre-exponentiële factor en Eact de
⎝ RT ⎠
activeringsenergie.
Katalysator efficiëntie
Katalysatorefficiëntie wordt uitgedrukt a.d.h.v. het turnover number, dit is het aantal gevormde
moleculen van het product door 1 katalysator voordat de katalysator gedeactiveerd wordt:
snelheid • levensduur katalysator
TON =
aantal katalysatoren
TON
Als je wil weten hoe snel de katalysator is bekijk je de turnover frequency, TOF =
tijd
Bij enzymen geldt dat TON = TOF en dit is maximaal kcat = k2 . De normale ‘TON' heet dan het
total turnover number (TTN).
Oorzaken van katalysator deactivering zijn:
- Dimerisering (homogene katalyse)
- Beschadiging van de katalysator door pH-verandering, oxidatie of temperatuur (voornamelijk bij
biokatalyse)
- Katalysator ontmenging bij gebruik van een legering of complex (heterogene katalyse)
- Katalysatorvergiftiging, intermediairen die niet meer loskomen van de katalysator (heterogene
katalyse)
Reactiemechanismen
Simple reaction Reactie die verloopt volgens 1 elementaire stap
Complex reaction Reactie die verloopt volgens ≥2 elementaire stappen
Als er nog een andere stof bindt aan de katalysator die de katalysator vervuilt (omdat die niet door
reageert) is er sprake van competitive inhibition.
De snelheidsbepalende stap is de stap die gaat over het hoogste punt in het energielandschap.
De snelheidsbepalende stap is niet per definitie de stap met de laagste snelheidsconstante, er
kunnen meer/minder reactanten zijn.
De selectiviteit van een reactie kan m.b.v. een katalysator bepaald worden voor alle stappen na de
snelheidsbepalende stap.
Principe van Sabatier
De beste katalysator bindt het belangrijkste katalytische intermediair niet te
sterk en niet te zwak. Bij een te sterkte binding reageert het intermediair niet
verder tot het product omdat het aan het oppervak blijft zitten terwijl bij een te
zwakke binding de katalysator niet goed aan de katalysator blijft zitten
waardoor de katalysator weinig effect heeft. Een meer negatieve
bindingssterkte is een sterke binding, dus links is te hard gebonden en rechts
te zacht.
Pagina 3 van 14