Hoorcollege 12 & 13: Eiwitten
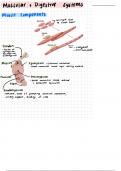
Eiwitten worden gepolymeriseerd; bestaat uit een reeks aminozuren die gekoppeld zijn.
Aminogroep & COOH groep aan de uiteinden. (Een links, een rechts)
Aminozuren worden gekoppeld doormiddel van een peptidebinding; vorming is belangrijk
Hier wordt water bij verbruikt. (OC-NH = peptidebinding)
Schrijfwijze: N-terminus naar C-terminus. (Aminogroep, COOH groep)
Eiwitten zijn polypeptide ketens, flexibiliteit wordt bepaald door de zijgroepen van de aminozuren.
Zijgroepen zijn belangrijk; kunnen reactief zijn (interactie met de omgeving, zuren, basen, afhankelijk
van pH omgeving.) Ook kunnen de OH groepen van tyrosine reageren met de omgeving.
Zijgroepen zijn bepalend voor de functie van eiwitten.
Functie eiwitten
Veel verschillende functies en 3D structuren.
• Enzymen
• Motoreiwitten
• Genregulatoren
• Hemoglobine (transport zuurstof)
De structuur van een eiwit bepaalt welk substraat het kan vervoeren/opnemen.
Alles wat eindigt op -ase is een eiwit.
Variabelen die de structuur en werking van een eiwit bepalen:
• De omgeving
• De aminozuursamenstelling en volgorde
• De secundaire en tertiaire structuur
• De post-translationele modificaties
• Binding van andere moleculen
1. De omgeving
Eiwitten in een waterige omgeving in de cel
65% van het menselijk lichaam bestaat uit water.
Water heeft het grootste effect in de cel op zwakke interacties
Zwakke interacties zijn benodigd voor:
• Dynamiek van moleculen in de cel
• Interactie tussen eiwitten
• Overbrengen van energie van ene naar andere molecuul
Niet-covalente reacties vormen en verbreken spontaan en snel.
Biomedische wetenschappen – Cellen
, XXXI
Eigenschappen water:
1. Eenvoudige samenstelling
2. Elektrische dipool (O = elektronegatief, H = elektropositief)
3. Is donor en acceptor voor het maken van waterstofbruggen
a. Donor: Het molecuul dat een H ‘afstaat’
b. Acceptor: Het molecuul dat een binding met het H-atoom aan gaat.
• Grote oppervlakte spanning
• Zeer hoog kookpunt (100C)
• Dynamisch: levensduur H-brug is 10-10 seconden -> Kookpunt is daarom 100C
Uitstekend oplosmiddel voor polaire stoffen
• Biologische moleculen (-fosfaat, amino-, -carboxyl)
• Organische moleculen (-hydroxyl, -sulfhydryl, -carbonyl)
• Zouten (Watermantel)
Water neemt deel aan chemische reacties in de cel.
Zuren en basen
Een zuur staat een proton (H+ ) af (dissociatie)
• Zwak zuur (Evenwichtsreactie)
• Sterk zuur (Aflopend)
Een base neemt een proton (H+) op (associatie)
• Zwakke base (Evenwichtsreactie)
• Sterke base (Aflopend)
Beide afhankelijk van de pH van de omgeving.
Stel:
HA <-> H+ + A-
pH KA /Kz
pH zegt iets over de H3O+ concentratie van een oplossing. ( pH = - log [H+] )
Is op te schrijven als een evenwichtsvergelijking:
Keq = ([H+] x [A-])/ [HA] → pKA = -log KA (pKA is een constante, die uniek is voor elk zuur/base)
(Blz 41, 42 (Blokboek/Alberts?))
Keq = ([H+] x [A-])/ [HA] → pH = pK + log [A-] / [HA]
• Evenwicht wordt sterk beïnvloed door [H+], en dus door pH
• 50% dissociatie: [A-] = [HA] ([A-] / [HA] = 1, log 1 = 0) pH = pK
o (Henderson-Hasselbalch vergelijking)
Belangrijk: Werkcollege 2 bekijken
Als pH > pK dan zal een zuur negatief geladen worden. Als pH = pK (+ 1 en -1 marge) dan 50/50
lading. Maar hij zal nooit positief worden; neutraal of negatief.
Als pH < pK dan zal een base positief geladen worden. Als pH = pK (+1 en -1 marge) dan 50/50
lading. Maar hij zal nooit negatief worden; neutraal of positief.
Biomedische wetenschappen – Cellen