7.1 Lewisstructuren
Water is een gebogen molecuul. Om te snappen waarom dat zo is, moet je eerst de Lewistheorie kennen:
Het eerste deel gaat over de edelgasconfiguratie en de covalentie. Niet allleen bij het vormen van
bindingen, maar ook bij de ruimtelijke molecuulbouw zijn valentie-elektronen bepalend.
In een structuurformule:
○ gedeeld elektronenpaar → aangegeven met streepje (binding)
○ vrij elektronenpaar → aangegeven met twee puntjes / een streepje
Het kan zijn dat in een Lewisstructuur een atoom meer of minder atoombindingen vormt dan je
volgens de covalentie zou verwachten. Toch kan dit nogsteeds een stabiel deeltje opleveren,
omdat alle atomen de edelgasconfiguratie bezitten. Wel krijgt het atoom een nettolading: De
formele lading = aantal valentie-elektronen — aantal elektronen dat zich op het atoom bevindt.
Hierbij telt een atoombinding altijd voor 1 elektron en is de lading nooit meer dan +1 of -1.
Soms kunnen er van een molecuul meerdere Lewisstructuren opgesteld worden. Degene met de minst
formele ladingen is de stabielste. De verschillende Lewisstructuren heten mesomere grensstructuren:
7.2 Ruimtelijke bouw
Een Lewisstructuur geeft genoeg informatie om een nauwkeurige voorspelling te doen van de ruimtelijke
bouw van een molecuul. De aanwezigheid van vrije elektronenparen is hierbij van grote invloed.
Bij de VSEPR-methode (Valence Shell Electron Pair Repulsion) gaan ze er vanuit dat elektronen elkaar
afstoten; de elektronen zullen zich dus zo verdelen dat ze zo ver mogelijk van elkaar af staan. Elektronen
bevinden zich altijd in paren die samen één positie innemen. Dit geldt ook voor de elektronenparen in een
(drie)dubbele binding.
Omringingsgetal = het aantal posities rond een atoom. Het is de som van het aantal bindingen plus het
aantal niet-bindende elektronenparen rond het centrale atoom. (Drie)dubbele bindingen tellen als één
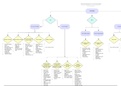
binding (elektronenpaar). Het omringingsgetal bepaalt of de bouw van het molecuul, zie schema:
Omringingsgetal 2 → lineaire bouw. Ideale hoek = 180°
Omringingsgetal 3 → vlakke bouw. Ideale hoek = 120°
Omringingsgetal 4 → tetraëdische bouw. Ideale hoek = 109,5°