HOOFDSTUK 8: DE ADAPTIEVE IMMUUNRESPONS IN TIJD EN RUIMTE
1/ Homeostasis: gedrag van immuuncellen VOORaleer ze in contact komen met hun cognate Ag
Naieve lymfocyten vinden hun specifiek Ag doordat ze circuleren tussen secundaire en tertiaire lymfoide weefsels:
• Vanuit bloed naar weefsel migreren : constant scannen naar Ag
• Organisatie van secundair lymfoide organen doen kans ↑
• Circulatie bloed-lymfeknoop-perifere weefsel en terug = 1-2x/dag
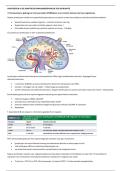
Circulatie van lymfocyten in een ‘rustende lymfeknoop’
Lymfocyten verlaten het bloed door extravasatie thv HEVs (high-endotheliale venulen) → geregeld door
adhesiemoleculen:
• L-selectine (CD62L) op naieve lymfocyten herkennen adressines van HEVs
• Contact : vertragen van de cellen + rollen langs de vaatwanden
• verder interacties met adhesiemoleculen: stoppen lymfocyten en persen zich door tussen de cellen = extravasatie
Extravasatie gestuurd door opeenvolgende activering van oppervlakte moleculen:
1. rollen/vertragen: CD62L-GlyCAM
2. activatie door chemokines op endotheelcellen-CCR7
3. arrest en adhesie door interactie integrines-Ig family members (ICAM) → autotaxin
4. diapedese
T-dependente B cel respons: chemokine geleide B cel migratie
Milt: extravasatie gestuurd door opeenvolgende activatie van opp-moleculen:
• lymfocyten via verschillende homing-mechanismen binnen in witte pulpa vd milt
• milt heeft geen HEVs en selectines spelen geen rol
• via arteriolen komen immuuncellen rechtstreeks in de marginale sinus
Naieve lymfocyten zoeken naar cognate Ag binnen reticulaire netwerken vd lymfeklier (en ook milt) → verschillen in
expressie van chemokine/ chemokinereceptoren resulteren in migratie van cellen
• T-cel zone : CCL21 en CCL19 tot expressie → naieve CCR7+ T cellen worden aangetrokken
, o Paracortex-LN, PALS-milt
• Folliculaire DC-netwerken: CXCL13 tot expressie → naieve CXCR5+ B cellen
o B cel follikels
Als lymfocyten hun cognate Ag niet in lymfeklieren kunnen vinden → S1P1-receptor → verlaten medullaire sinus via
efferente lymfevaten → terug naar bloedsomloop
2/ Immuunrespons bij contact met een Ag
Ag wordt herkend door cellen vh AANGEBOREN immuunsysteem:
• Aangeboren immuuncellen (oa monocyten, macrofagen, …) bindenpathogenen via PPRs (patroon-recognitie-
receptoren vb TLR)
• PRR-binding genereert signalen die resulteren in secretie van ontstekingssignalen (chemokines en cytokines)
o Type TLR bepaald verdere immuunrespons
• Chemokines trekken innate immuuncellen aan naar plaats van infectie
• Neutrofielen reageren als eerste op chemokine-aantrekking en produceren meer chemokinen die APCs en DCs
aantrekken
Ag komen in 2 verschillende vormen aan in secundair lymfoide weefsel via afferente lymfevaten:
1. APC op de plaats van infectie nemen Ag op → presenteren een verwerkt peptide in een MHC molecule
Upregulatie van chemokinereceptoren die drainerende LN brengen = start adaptieve immuunrespons
2. Ag gaan direct naar de lymfeknoop → worden herkent en verwerkt door APC in de lymfeknoop
Hoe vinden APC die Ag hebben verwerkt hun weg naar plaats van circulerende T cellen (= T cel zone in lymfeknoop/milt)
• Geactiveerde APC verwerken Ag en upreguleren CCR7
o Endotheelcellen in lymfevaten brengen CCL21 tot expressie
o Lymfeknoop: APC nestelt langs FRC circuits in paracortex (stromale cellen bron van CCL21)
• APC gaat op zoek naar T cellen met juiste TCR in de paracortex
Hoe vinden onverwerkte Ag hun weg naar de plaats van circulerende B cellen (= B cel zone)
• Lymfeklier:
o Oplosbaar Ag kan lymfeklier binnendringen vanuit bloed of via afferente lymfevaten
o Kleine en grote Ag eindigen in subcapsulaire sinus
, o CD169+ macrofagen in subcapsulaire sinus transfereren met complement geopsoniseerde Ag of Ag-Ab-
complexen naar cellen in lymfeklier (nonAg specifieke B cellen, macrofagen → FDC)
• Milt:
o Blood-borne Ag worden gevangen door gespecialiseerde APC in marginale zone vd milt
o Ag komt rechtstreeks vanuit bloed
o Onverwerkt Ag doorgegeven aan follikels door macrofagen die de sinus van de marginale zone bekleden
o Verwerkt Ag wordt door APC naar de T cel zone gebracht
Primaire immuunrespons in de lymfeklier: gedrag van T cel, B cel en APC tijdens de eerste 50u
• Naieve CD4+ cellen stoppen hun bewegingen na binding van hun cognate Ag: T-cel activatie en differentiatie
• CD8+ T cellen geactiveerd in lymfeklieren via een meercellige interactie (CD4-APC-CD8)
o Binding met MHC klasse 1-Ag op een APC → partiele activatie van CD8+ T cel
o Nood aan CD4+ T cel hulp voor optimale differentiatie + voor generatie van geheugencellen
• B cellen zoeken hulp van CD4+ T cellen op de grens tussen follikel en paracortex vd lymfeklier
o Na binding van Ag zullen B cellen CCR7 upreguleren : chemotactische signalen volgen naar paracortex
o T helper cellen aangetrokken naar follikelrand (upregulatie van CCR5 na activatie)
o T cel/B cel interacties aan follikelgrens
Gedrag van immuuncellen tijdens de ADAPTIEVE immuunrespons:
B cel activatie → B cel proliferatie en differentiatie naar plasmacellen, geheugen B cellen en vorming van germinale centra
• Lichte zone: beperkte aantal B cellen, TFH en folliculaire DCs → plaats waar affiniteit van BCR voor Ag getest wordt
→ plasma- en geheugenceldifferentiatie
• Donkere zone: plaats van proliferatie en SHM (somatische hypermutatie)
• GC TFH zijn mobiel en verlenen hulp binnen verschillende GC
• Hoogste affiniteit voor Ag B cellen domineren de GC
EINDE van de immuunrespons: contraheert na 10-14 dagen: nadat Ag is verwijderd, zijn meeste lymfocyten niet langer
nodig en zullen ze afsterven door apoptose:
, 1. Aan einde van infectie is er minder Ag en zijn er bijgevolg minder stimulerende cytokines (IL-2, IL-7, IL-15) →
apoptose van immuuncellen
2. T cellen en sommige APC brengen Fas tot expressie + geactiveerde T cellen brengen FasL tot expressie → AICD =
activation induced cell death → T-cel expansie wordt gelimiteerd
3. Late fase van immuunrespons zullen geactiveerde lymfocyten ook negatieve co-stimulatoire eiwitten upreguleren
(CTLA-4 en PD-1)
4. Regulatoire cellen kunnen ook helpen om reacties te onderdrukken door secretie van inhiberende cytokines
Geactiveerde lymfocyten (= effectorcellen) verlaten de lymfeklier en recirculeren door verschillende weefsels
• Plasmacellen naar verschillende locaties:
o Vroege IgM-producerende plasmacellen: naar medulla van lymfeklier (release van Ab in efferente
lymfevaten)
o IgG-producerende: naar beenmerg
o IgA-producerende: naar MALT (mucosal-associated lymphoid tissue) vooral in darm
• Effector en geheugen T cellen naar organen en infectieplaatsen
o Volgen chemokine-gradiënten die worden gegenereerd door innate immuunreactis in die gebieden
• Memory cellen scheiden zich van effectorcellen na 9-10 delingen
o Centraal geheugen T cellen = TCM = blijven in secundair lymfoide weefsel
o Effector geheugen T cellen = TEM = circuleren tussen perifere weefsels
o Weefsel-residente geheugen T cellen = TRM = langdurig resident in barriereweefsel en vormen IELs (intra-
epithelial lymfocyt) van darm en huid
Chemokine receptoren en adhesie moleculen reguleren homing van effector en memory lymfocyten naar de perifere
weefsels
HOOFDSTUK 9: EFFECTOR FUNCTIES
1/ Antistof-gemedieerde immuniteit (extracellulaire pathogenen)
1/ Homeostasis: gedrag van immuuncellen VOORaleer ze in contact komen met hun cognate Ag
Naieve lymfocyten vinden hun specifiek Ag doordat ze circuleren tussen secundaire en tertiaire lymfoide weefsels:
• Vanuit bloed naar weefsel migreren : constant scannen naar Ag
• Organisatie van secundair lymfoide organen doen kans ↑
• Circulatie bloed-lymfeknoop-perifere weefsel en terug = 1-2x/dag
Circulatie van lymfocyten in een ‘rustende lymfeknoop’
Lymfocyten verlaten het bloed door extravasatie thv HEVs (high-endotheliale venulen) → geregeld door
adhesiemoleculen:
• L-selectine (CD62L) op naieve lymfocyten herkennen adressines van HEVs
• Contact : vertragen van de cellen + rollen langs de vaatwanden
• verder interacties met adhesiemoleculen: stoppen lymfocyten en persen zich door tussen de cellen = extravasatie
Extravasatie gestuurd door opeenvolgende activering van oppervlakte moleculen:
1. rollen/vertragen: CD62L-GlyCAM
2. activatie door chemokines op endotheelcellen-CCR7
3. arrest en adhesie door interactie integrines-Ig family members (ICAM) → autotaxin
4. diapedese
T-dependente B cel respons: chemokine geleide B cel migratie
Milt: extravasatie gestuurd door opeenvolgende activatie van opp-moleculen:
• lymfocyten via verschillende homing-mechanismen binnen in witte pulpa vd milt
• milt heeft geen HEVs en selectines spelen geen rol
• via arteriolen komen immuuncellen rechtstreeks in de marginale sinus
Naieve lymfocyten zoeken naar cognate Ag binnen reticulaire netwerken vd lymfeklier (en ook milt) → verschillen in
expressie van chemokine/ chemokinereceptoren resulteren in migratie van cellen
• T-cel zone : CCL21 en CCL19 tot expressie → naieve CCR7+ T cellen worden aangetrokken
, o Paracortex-LN, PALS-milt
• Folliculaire DC-netwerken: CXCL13 tot expressie → naieve CXCR5+ B cellen
o B cel follikels
Als lymfocyten hun cognate Ag niet in lymfeklieren kunnen vinden → S1P1-receptor → verlaten medullaire sinus via
efferente lymfevaten → terug naar bloedsomloop
2/ Immuunrespons bij contact met een Ag
Ag wordt herkend door cellen vh AANGEBOREN immuunsysteem:
• Aangeboren immuuncellen (oa monocyten, macrofagen, …) bindenpathogenen via PPRs (patroon-recognitie-
receptoren vb TLR)
• PRR-binding genereert signalen die resulteren in secretie van ontstekingssignalen (chemokines en cytokines)
o Type TLR bepaald verdere immuunrespons
• Chemokines trekken innate immuuncellen aan naar plaats van infectie
• Neutrofielen reageren als eerste op chemokine-aantrekking en produceren meer chemokinen die APCs en DCs
aantrekken
Ag komen in 2 verschillende vormen aan in secundair lymfoide weefsel via afferente lymfevaten:
1. APC op de plaats van infectie nemen Ag op → presenteren een verwerkt peptide in een MHC molecule
Upregulatie van chemokinereceptoren die drainerende LN brengen = start adaptieve immuunrespons
2. Ag gaan direct naar de lymfeknoop → worden herkent en verwerkt door APC in de lymfeknoop
Hoe vinden APC die Ag hebben verwerkt hun weg naar plaats van circulerende T cellen (= T cel zone in lymfeknoop/milt)
• Geactiveerde APC verwerken Ag en upreguleren CCR7
o Endotheelcellen in lymfevaten brengen CCL21 tot expressie
o Lymfeknoop: APC nestelt langs FRC circuits in paracortex (stromale cellen bron van CCL21)
• APC gaat op zoek naar T cellen met juiste TCR in de paracortex
Hoe vinden onverwerkte Ag hun weg naar de plaats van circulerende B cellen (= B cel zone)
• Lymfeklier:
o Oplosbaar Ag kan lymfeklier binnendringen vanuit bloed of via afferente lymfevaten
o Kleine en grote Ag eindigen in subcapsulaire sinus
, o CD169+ macrofagen in subcapsulaire sinus transfereren met complement geopsoniseerde Ag of Ag-Ab-
complexen naar cellen in lymfeklier (nonAg specifieke B cellen, macrofagen → FDC)
• Milt:
o Blood-borne Ag worden gevangen door gespecialiseerde APC in marginale zone vd milt
o Ag komt rechtstreeks vanuit bloed
o Onverwerkt Ag doorgegeven aan follikels door macrofagen die de sinus van de marginale zone bekleden
o Verwerkt Ag wordt door APC naar de T cel zone gebracht
Primaire immuunrespons in de lymfeklier: gedrag van T cel, B cel en APC tijdens de eerste 50u
• Naieve CD4+ cellen stoppen hun bewegingen na binding van hun cognate Ag: T-cel activatie en differentiatie
• CD8+ T cellen geactiveerd in lymfeklieren via een meercellige interactie (CD4-APC-CD8)
o Binding met MHC klasse 1-Ag op een APC → partiele activatie van CD8+ T cel
o Nood aan CD4+ T cel hulp voor optimale differentiatie + voor generatie van geheugencellen
• B cellen zoeken hulp van CD4+ T cellen op de grens tussen follikel en paracortex vd lymfeklier
o Na binding van Ag zullen B cellen CCR7 upreguleren : chemotactische signalen volgen naar paracortex
o T helper cellen aangetrokken naar follikelrand (upregulatie van CCR5 na activatie)
o T cel/B cel interacties aan follikelgrens
Gedrag van immuuncellen tijdens de ADAPTIEVE immuunrespons:
B cel activatie → B cel proliferatie en differentiatie naar plasmacellen, geheugen B cellen en vorming van germinale centra
• Lichte zone: beperkte aantal B cellen, TFH en folliculaire DCs → plaats waar affiniteit van BCR voor Ag getest wordt
→ plasma- en geheugenceldifferentiatie
• Donkere zone: plaats van proliferatie en SHM (somatische hypermutatie)
• GC TFH zijn mobiel en verlenen hulp binnen verschillende GC
• Hoogste affiniteit voor Ag B cellen domineren de GC
EINDE van de immuunrespons: contraheert na 10-14 dagen: nadat Ag is verwijderd, zijn meeste lymfocyten niet langer
nodig en zullen ze afsterven door apoptose:
, 1. Aan einde van infectie is er minder Ag en zijn er bijgevolg minder stimulerende cytokines (IL-2, IL-7, IL-15) →
apoptose van immuuncellen
2. T cellen en sommige APC brengen Fas tot expressie + geactiveerde T cellen brengen FasL tot expressie → AICD =
activation induced cell death → T-cel expansie wordt gelimiteerd
3. Late fase van immuunrespons zullen geactiveerde lymfocyten ook negatieve co-stimulatoire eiwitten upreguleren
(CTLA-4 en PD-1)
4. Regulatoire cellen kunnen ook helpen om reacties te onderdrukken door secretie van inhiberende cytokines
Geactiveerde lymfocyten (= effectorcellen) verlaten de lymfeklier en recirculeren door verschillende weefsels
• Plasmacellen naar verschillende locaties:
o Vroege IgM-producerende plasmacellen: naar medulla van lymfeklier (release van Ab in efferente
lymfevaten)
o IgG-producerende: naar beenmerg
o IgA-producerende: naar MALT (mucosal-associated lymphoid tissue) vooral in darm
• Effector en geheugen T cellen naar organen en infectieplaatsen
o Volgen chemokine-gradiënten die worden gegenereerd door innate immuunreactis in die gebieden
• Memory cellen scheiden zich van effectorcellen na 9-10 delingen
o Centraal geheugen T cellen = TCM = blijven in secundair lymfoide weefsel
o Effector geheugen T cellen = TEM = circuleren tussen perifere weefsels
o Weefsel-residente geheugen T cellen = TRM = langdurig resident in barriereweefsel en vormen IELs (intra-
epithelial lymfocyt) van darm en huid
Chemokine receptoren en adhesie moleculen reguleren homing van effector en memory lymfocyten naar de perifere
weefsels
HOOFDSTUK 9: EFFECTOR FUNCTIES
1/ Antistof-gemedieerde immuniteit (extracellulaire pathogenen)