Duaal karakter
LEREN
- Onderzoek van een oplossing gebeurt met de complementaire kleur van de oplossing
Een blauwe oplossing wordt onderzocht met oranje
- Verschijnsel van absorptie en emissie
Elektron absorbeert een foton komt in aangeslagen toestand
Bepaalde golflengten bij voorkeur
Elektron gaat terug naar de grondtoestand
Er kan een foton worden uitgezonden
De energie kan omgezet worden in warmte
De molecule kan een fotochemische reactie ondergaan
,a = transmissie dor de ‘eenheidsweglengte’
, - Extinctie E (Absorbance A): het geabsorbeerde licht
It/I0 %T E
1 100 0
0,1 10 1
0,01 1 2
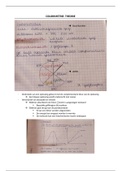
IJklijnen bij spectrofotometrie
Concentratie blijft constant, maar weglengte verandert (geen goede methode)
Weglengte blijft constant, maar concentratie verandert (juiste methode)
- Extinctiecoëfficiënt: altijd het grootste bij λmax
Golflengte < λmax: constante rechte ligt onder λmax
Golflengte > λmax: constante rechte ligt ook onder λmax
- Extinctiecurve
λmax wordt duidelijk afleesbaar
Wet van Lambert-Beer is enkel geldig bij zeer verdunde oplossingen
1. Praktische uitvoering van een colorimetrische bepaling
, 1.1. Algemeen schema
- Uit het lichtspectrum van de lamp wordt 1 golflengte geselecteerd
Monochromatisch licht gaat door de oplossing
Intensiteit van de uittredende straal (T) wordt gemeten
Geabsorbeerde licht (E) wordt berekend
1.2. De cuvet
- Balkvormig buisje dat men kan wegwerpen, altijd 1 cm (weglengte l = 1 cm)
- Blanco: alle stoffen uit het monster, behalve degene die wordt getest
Reflectie van cuvetwand is niet te verwaarlozen
Soms kunnen toegevoegde reagentia ook absorberende eigenschappen hebben
Voor elke meting gebruikt men de blanco om de meter op 0,000 te zetten
1.3. Samenstelling van de blanco
- Alle stoffen uit het monster, buiten de stof die wordt getest (reagens- of monsterblanco)
Meetwaarde van blanco = x (meestal 0,000 via meter)
Meetwaarde van monster = y
E=y–x
1.4. De golflengte instellen
1.4.1. Waarom is λmax zo belangrijk?
- dE/dc is maximaal verandering van c geeft grootste verandering van E
Concentratie kan zeer nauwkeurig bepaald worden (grootste gevoeligheid)
De fout op de waarde is het kleinst
- Bij deze golflengte is de verandering van E minimaal kleine verandering van λ is
verwaarloosbaar
1.4.2. Extinctiecurve maken
- Voor elke meting wordt E op 0,000 gezet met de blanco
- Met de meest geconcentreerde standaardoplossing wordt het golflengtegebied doorlopen
700nm tot 400nm met stappen van 20nm
Rond het maximum met stappen van 2 à 5 nm
- Zet alle waarden uit op een grafiek (E ifv λ)
1.5. De ijklijn
- De golflengte wordt niet meer aangepast eenmaal op 0,000 zetten met blanco
Alle standaardoplossingen worden gemeten
De waarden worden uitgezet op een grafiek (E ifv c is door de oorsprong)
- Nauwkeurigheid testen
Men werkt met E tussen 0,100 en 1,500
De concentratie van de onbekende zit tussen de standaarden
1.6. Bereiding van standaardoplossingen
- Er wordt een verdunningstabel gemaakt
Beginconcentratie is altijd 100 ppm